Az arzén oxidációjának foka: az arzén kémiai tulajdonságai
Mielőtt figyelembe vesszük az oxidációs állapototarzén, megmutatjuk pozícióját az időszakos táblában és a szerkezet jellemzőiben. Ezenkívül nevezzük meg ennek a kémiai elemnek az alapvető fizikai és kémiai tulajdonságait.

Pozíció a PS-ben
Az arzén, a vegyi anyag fő oxidációs állapotatulajdonságok, alkalmazás - mindezt megtanulhatjuk, ha megvizsgáljuk a Mendeleev periodikus rendszer elemének helyét. Arzén található az ötödik csoportban, a fő alcsoport, tagja a nitrogén családnak. Relatív atomtömege 74,9216. Az arzén oxidációjának főbb fokai pontosan arra a csoportra vonatkoznak, amelyben az SS található. Ez az elem 33 sorszámmal rendelkezik. Az energiaszintek száma megfelel annak a periódusnak a számához, amelyben az elem található, négyszerese.
Vegye figyelembe az elektronok elrendezésétatomhéj. Az első energiaszintben csak két csatolt elektron van, a második héj nyolc részecske: 2s és 6p. A harmadik szinten, eltekintve tőlük, tíz d-elektron van, vagyis csak 18 részecskék. A külső energia szint egy 2s-elektron, valamint három párosítatlan p-elektron. Ez a valence elektronok száma, amely meghatározza az arzén oxidációjának lehetséges fokát.
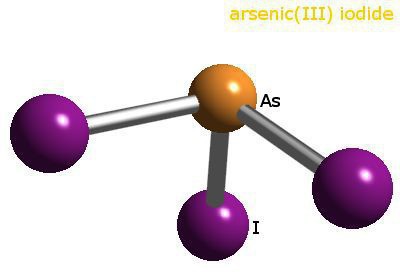
Történeti oldalak
Arsenik az öt "alkímiai"a középkorból ismert elemek. Érdekesség az, hogy négy az ötödik PS csoportban van. Akkoriban senki nem tudta meghatározni az arzén oxidációjának mértékét, de a vegyületeket sikeresen alkalmazták gyógyszerek előállítására, festékek előállítására.
Miután a kőkorszakot a bronzkori korszakra cserélték, az emberekmegtanulták, hogyan lehet ezt az ötvözetet különleges tulajdonságokkal ellátni. Kiderült, hogy az arzén 7 százalékát és az ón 3 százalékát tartalmazta. A tudósok úgy vélik, hogy az első, a bronz helyett a malachit helyett, ami zöld, tévesen vette át a réz-arzén ásványi anyagok zöld szulfidjait.
A kapott ötvözet csodálatos teljesítménye népszerűvé vált az ősi mesterek körében. Különösen az anyagot tartalmazó ásványi anyagokat keresték.
Arzén oxidációs foka ilyen vegyületekbentipus pozitív, megfelel a magasabb valenciának. Az arzént tartalmazó szulfidok azonosítása céljából az ásványi anyagot felmelegítik. Egy adott fokhagyma illata megjelenése megerősíti az arzén jelenlétét a vegyületben. Fokozatosan az olvasztás az arzen bronz elutasította. A termelés megszűnésének okai között a tudósok a munkák folyamatos mérgezését nevezik a mestereknek.

Természetes ásványok
Ásvány formájában, az általunk vizsgált anyagaz ősi idők óta ismert. Például a 3-arzén oxidációs állapota az ókori Kínában ismert vegyületként jelenik meg, mint "bánya por". Arisztotelész leírta az ásványi szandarakot, amely arzén-szulfid. A latin nyelvből lefordítva a neve aranyszínű festéknek hangzik. Ezekben a távoli időkben sárga festékként használták.
A tizenegyedik században alkimistákkülönböző anyagokat tartalmaz. Az arzén oxidációjának fokozata a felsorolt vegyületekben a csoport számához igazodik. A fehér arzén hatvegyértékű oxidnak nevezte, a sárga szulfidnak nevezték, és vörös - As4S4 (tetrasulfid tetrashyyyaka).
A fehér változatot a szennyeződések szublimációjával nyertüka rézércek égetésének folyamata, amely arzént tartalmazott. A gázállapotból származó kondenzáció miatt az arzén-oxid fehér színű lerakódásként csapódik ki. Az ősi idők óta használják a kártevők elpusztításának eszközeként.
A tizenharmadik században Nagy Albertegy fém anyagot kapunk. A sárga arzént szappannal melegítette fel. Az interakció eredményeként kapott anyag nem erősítette meg a hét fém és a bolygók misztikus kapcsolatát. Talán ez annak köszönhető, hogy az ellentmondások által feltárt ősi alkimisták arzén tekinthető „illegitim” elem. Ez volt akkoriban kiderült, a képesség, hogy ruházza réz fehér, így vált ismertté, mint egy olyan „fehéredés Venus”.
Ez egy egyedi anyaga kémiai elemet csak a tizenhetedik század közepén azonosította. A német gyógyszerész, Johann Schröder sikeresen elkülönítette a kőszén-oxidok kémiai redukcióját. Nichola Lemery egy idő után sikerült kivonnia a fémeket kálium, szappan, arzén-oxid melegítésével. A 18. században ez a fém szokatlan "félvezető" volt.
A XVIII. Század végén a svéd kémikus K.V. A Scheele arzénsavat eredményezett, amelyben az arzén legmagasabb oxidációs szintje: +5. A tizenkilencedik században az arzént tartalmazó szerves anyagokat azonosították.

A természetben
Az arzén legmagasabb és legalacsonyabb oxidációjatermészetes vegyületekben nyilvánulnak meg. A Föld kéregében ez az elem százalékos koncentrációja nem haladja meg az 5 grammot tonnánként. Sok ásványi anyagban egyidejűleg tartalmaz nikkelt, kobaltot, rézöt, vasat.
Jelenleg körülbelül kétszázkülönböző természetes ásványi anyagokat, amelyek magukban foglalják a kémiai elemet, amelyet mérlegelünk. Tekintettel arra, hogy az arzén oxidációjának magasabb és alacsonyabb szintjét mutatják, más alkalmazással rendelkeznek. Például antimonnal kombinálva az arzén negatív oxidációs állapotot mutat. Tekintettel arra, hogy ez a fém alacsony elektronegativitást mutat, a legalacsonyabb arzén oxidációs foka -3. Ez az indikátor az arsenidekre és az ásványi almontitra jellemző.
A legtöbb vegyületek fémekkel arzén, sajátosságára a készítmény, egy intermetallikus vegyület, azzal jellemezve, összetételének a változtatásával a kémiai elem.
Az arsenidek jellemzői
Az arsenideket többféle tartalom jellemzia kristályrácsok hasonló szerkezetével rendelkező fémek. Ezeket az ásványi anyagokat fémes fény jellemzi, átlátszatlanak, kis keménységűek.
A természetes arzenidek példájaként a következő vegyületeket lehet figyelembe venni:
- lellingite, hasonló a pirithoz;
- nikkel, amelyet nikkel piros piritnak neveznek;
- langisit;
- Oregon;
- sperrylite.
Ez természetesen nem teljes listahasonló ásványi anyagok - jelenleg körülbelül húsz ilyen vegyület. A leggyakoribb természetűek közül említhetjük az arzénpiritet, az arzén-piritot. Ez egy olyan termék, amelyet a piritban található kénatomok arzénnel való helyettesítésével kapunk. Az ilyen vegyületeket, amelyekben az arzén legmagasabb oxidációs szintje nem nyilvánul meg, szulfoszálokat neveznek.
Analógjaik a kobalt fényét tekintik,gersdorfit, enargit és proustit. Ez utóbbi fontos ezüstérc, amely a drágakő felső rétegében helyezkedik el. A szulfoszálok összetétele lehet a platinacsoport nemesfémjei. Közülük érdeklődést jelent az iráziusz, valamint az orsit. Összetételük szerint ritka fémek kiváló szerves és szervetlen szintézissel katalizátorként használhatók fel.
Az arzén oxidációjának maximális mértékéta természetes szulfidokban nyilvánul meg. Például a narancssárga dimorfitban, ami az arzén-szulfid (5). A harmincas években a múlt század, természetes lelőhelye orpiment, beleértve a tagság szulfid, trivalens arzén, a déli a Verhojanszki tartomány talált. Az észlelt kristályok mérete 60 centimétert ért el, és a súlyt 30 kg-ra becsültük.

Az arzenátumok jellemzői
Az arzén oxidációjának lehetséges foka lehetségesvegye figyelembe a sók példáját. Így az arzénsavaknak nevezett arzénsav vegyületek a fém maximális értékét mutatják: +5. Az ilyen vegyületek példájaként eritrinet adunk, amelynek fényes rózsaszín színe van. Ezt a sót kobalt színnek nevezik, a Co3 (AsO4) 2 * 8H képlettel jellemezhető2O. Meg lehet jegyezni a barnás-piros árnyalat gázrolitját is (Ce, La, Nd) ArO4.
Svédország központjában, a Langbanavas-mangán kőbányák, ahol mintegy ötven különböző arzenátumot találtak és jellemeztek. Ezeket a vegyületeket az arzénsav és a mangán-hidroxid (2) kölcsönhatása alacsony hőmérsékleten állítja elő.
Milyenek az oxidációs állapotok az arzenátumokban?Arzén? Ezeknek a sóknak a jellemzői megerősítik a kén jelenlétét. Annak ellenére, hogy nincsenek ipari alkalmazások, esztétikai megjelenésük lehetővé teszi számukra, hogy ásványtani gyűjteményeket hozzanak létre.
Érdekes történet a kupfernikel, amelymegfelel a nikkel ásványnak. Középkori német bányászok Nickel nevű hegyi gonosz szellem, és "hamis réz" nevezték "kupfernickel". A mesterek kiderítették, hogy az ásvány réz-vörös kristályai rézércekkel hasonlítanak. Üveg előállításához használták, így a kapott termék zöld színű volt. Csak a tizennyolcadik század közepén sikerült az ásványi anyagot kivonni az ásványból, Axel Kronstedt.
A természet jellegzetes szálláslehetőségei
Az arzént magas tehetetlenség jellemzi,így natív állapotban található. Hasonló összetételű fém két-tizenhat százalékos szennyeződéssel rendelkezik, főként ezüst, vas, kobalt, nikkel. Hazánkban a geológusok felfedezték a natív arzént az Amur régióban, a Transbaikáliában.
Megtalálható a kőzetek és ásványok, valamint a növényekben, ezért joggal gyakran nevezik a mindennapok elem.
Mi a maximális és legkisebb mértékaz arzén oxidációja? A legmagasabb érték megegyezik annak a csoportnak a számával, amelyben ez az elem található, és +5. Ez olyan vegyületekre jellemző, ahol redukáló tulajdonságokkal rendelkezik. Az egyedi fém összekapcsolásának részleteit később figyelembe veszik.
A földön az arzén rendkívül egyenetlen eloszlású. Ennek oka a lithosphere kialakulása, valamint az üledékes kőzetekben és talajokban előforduló deszorpciós és szorpciós folyamatok.
Ennek a fémnek a vízben való kiváló oldhatósága miatt könnyen vándorol. Például nedves klímában a talajból kimossák, majd a talajvízzel és a folyókkal együtt mozognak.

Fiziológiai hatás
Jelentős mennyiségben található az arzénásványvizek. Vannak bizonyos szabványok a fém tartalmára vonatkozóan. Ha a megengedett értékeket túllépik, az emberi szervezet súlyos veszélyt jelent. A kémiai vizsgálatok során megállapítottam, hogy az arzén a természetes vízben különféle formákban is megtalálható. Mi legyen az arzén oxidációs állapota? A vízben található vegyületek tulajdonságai megerõsítik a fém jelenlétét arzenio-savas oldatként.
Az arzén élő formában körülbelül 6 mg / lkg. A hínár egy része felhalmozhatja a fenti anyagot olyan mértékben, hogy veszélyes lehet az emberi test számára. Az ázsiai országokban talált fajok egy része tiszta savas oldatban képes szaporodni. A patkányok ellenőrzésére használják őket. Az emberi agyszövetben, valamint az izmokban elegendő mennyiségű fém van. Ezenkívül jelen van a körömlemezekben, felhalmozódik a hajban.
Fizikai jellemzők
Annak ellenére, hogy az arzén néz kifém, nem fémes tulajdonságokkal is rendelkezik. Például képtelen kénsavval sókat képezni, amely savképző elemként működik. Az arzén különböző allotropikus módosításokban létezhet, ami a foszforra emlékeztet. A legstabilabb a szürke arzén, amely fűtött állapotban, szublimes, mint a jód.
Az elektromos vezetőképesség, ez a módosítása rézhez jut, de meghaladja a higanyt. Hegesztés közben az arzéngőz lágy, áttetsző, sárga színárnyalatú anyagot kap, hasonlóan a sárga foszforhoz. A melegítés folyamán ez a kémiai elem egy másik allotropikus módosítása.
Amikor az arzéngőzöket üvegre helyezzük, megfigyelhetjük egy tükörfilm megjelenését.

Arzénvegyületek
Az arzén oxidációjának foka a magasabb oxidokban+5, vagyis nagyobb a valenciája. De egy adott fém nedves levegőben lévő gőzök szublimációjakor az arzén-anhidrid As2O3. Ebben a formában, főleg, ennek az elemnek egy oxidja van. Ez az oxid amfoter kémiai tulajdonságokkal rendelkezik.
Az oxidációs folyamatban magasabb oxiddá alakul, ahol az arzén az oxidációs fok +5 értékét mutatja.
A tiszta fémt hígított salétromsavval H orto-arzénsavvá oxidáljuk3AsO3, amelynek értéke 3. Kémiai képességei szerint közepes szilárd savnak tekinthető, hasonlóan a bórsavhoz. A sókat arzeniteknek tekintik, amelyek világos visszanyerési tulajdonságokat mutatnak.
A kloridban a fém oxidációs állapota +3,tipikus fémelemként működik. Az aktív fémekkel való kölcsönhatás során képződő só-arzenideket vizes hidrolízisnek vetjük alá. Például az arciin (AsH3) mérgező, színtelen gáz, szagtalan.
Szerves fémvegyületek
Az arzén különböző formákat képes kialakítanifémorganikus vegyületek. Például a 18. század végén, a kálium-acetát arzén-oxidja (3) lepárlásával kellemetlen szagú füstölő folyadékot kaptak. A kapott terméket alarsinnak neveztük el. A későbbi vizsgálatok során kimutatták, hogy arzént tartalmaz.
A tizenkilencedik század végén szintetizáltaromás arsinek. A reakciót arzén-triklorid és aril-halogenid és fém-nátrium keverékével való expozícióval végezzük. Néhány ilyen termék antimikrobiális tulajdonságot mutatott. Napjainkig több tízezer szerves klórvegyület szintézise folyik.
Arzén alkalmazása
A bányászott fémek több mint felekülönböző vegyületek formájában használják. Tiszta formájában gyakorlatilag nem használják. Kis mennyiségben beadják a csapágyötvözetekbe. Az ilyen adalékok pozitív hatást gyakorolnak a késztermék keménységére, ezért keresnek elektromos kábelek és elemek gyártása során.
A minimális arzén dózis hozzájárul a növekedéshezkorrózióálló, javítja a sárgaréz és réz hőteljesítményét. Ha ez az elem nem tartalmaz további szennyeződéseket, akkor a félvezető eszközök gyártása során van szükség. Ezek létrehozásához az arzént germániummal vagy szilíciummal fuzionálják.
Ezenkívül kiváló ötvözetadalékanyag az acélok létrehozásakor. Értékes fúvóként az arzént a színesfém-kohászat esetében is meg kell tenni. Még ha az ötvözetben alacsony a tartalma, jelentősen javítható a gyártott termék erőssége. Az arzén növeli a réz folyékonyságát az öntés során, megkönnyítve a huzal megszerzését.
Ez az átmeneti fém egy bizonyos negatív hatása a termelésre. Az ércben való jelenléte a folyamatot káros hatásúvá teszi.
A különböző érdekes arzénvegyületek közüljelentése háromértékű oxidja. Jelenleg üvegárukban használják. A +5-ös jelzőszámú sókat antiszeptikumokként kell felvenni. Ez az átmeneti elem a modern kémiai termelés egyik legkeresettebb, hiszen a folyamat környezetétől függően kettős tulajdonságokkal rendelkezik.
</ p>